Científicos de la División de Oncología Molecular y Traslacional del CIEMAT y pertenecientes al CIBERONC y al Instituto de Investigación Sanitaria Hospital 12 de Octubre (imas12), en colaboración con científicos de la Universidad de Santiago de Compostela, han desentrañado el papel oncogénico del gen ERAS en la glándula mamaria. El trabajo ha sido publicado en la revista Cancers.
Las proteínas RAS son una familia de proteínas encargadas de transmitir al núcleo celular las señales que las células reciben de su entorno, regulando de esta manera el crecimiento y diferenciación celular. No es de extrañar por tanto que alteraciones en la actividad de miembros de esta familia conduzcan con frecuencia a la formación de lesiones tumorales. De hecho, la vía de señalización de RAS está alterada en aproximadamente la mitad de los tumores humanos. ERAS (de Embryonic-RAS) es un miembro relativamente poco conocido de esta familia de genes RAS que se expresa tan solo durante el desarrollo embrionario temprano del individuo, siendo silenciado posteriormente en condiciones normales.
En este trabajo - coordinado por el investigador del CIBERONC Ángel Ramírez - se estudian las consecuencias que la expresión desregulada de ERAS tiene en fisiopatología de la glándula mamaria. Para ello, se obtuvieron líneas de ratones portadores de un transgén para la expresión de ERAS en las células basales de los epitelios estratificados y en las células mioepiteliales de glándula mamaria y otras glándulas exocrinas. Estos animales presentaron, además de alteraciones en el crecimiento de órganos y tejidos con expresión del transgén, alteraciones en el desarrollo y funcionamiento de la glándula mamaria.
Además de aparecer tumores en diversos tejidos epiteliales, las glándulas mamarias desarrollaron, con alta incidencia, carcinomas intraductales. El estudio histopatológico de estos tumores, así como el estudio de expresión de diversos marcadores de diferenciación, indicaron la gran similitud de los tumores de ratón causados por la sobreexpresión de ERAS con el tipo de tumor humano denominado adenomioepitelioma maligno, un tumor mamario relativamente raro.
Este equipo había detectado anteriormente que ERAS se expresa de forma aberrante en algunos tumores de mama humanos. En este estudio, se muestra que la expresión inadecuada de este gen es capaz, por sí sola, de producir tumores.
"En conjunto, este trabajo arroja luz sobre las consecuencias de la expresión desregulada de ERAS, y aporta luz sobre el posible origen de los adenomiepiteliomas malignos de mama en humanos" señalan los autores.
Este estudio se ha llevado a cabo en el CIEMAT/CIBERONC y en el Instituto de Investigación Sanitaria Hospital 12 de Octubre (imas12), y ha contado con la colaboración de investigadores de la Universidad de Santiago de Compostela
En este estudio se han utilizado animales de experimentación. Este uso ha sido autorizado por la autoridad competente conforme a la normativa vigente y se han respetado los máximos criterios de bienestar animal para la realización del mismo. Este trabajo ha sido posible gracias a las subvenciones obtenidas del Instituto de Salud Carlos III, cofinanciado por el Fondo Europeo de Desarrollo Regional (FEDER), así como por otras subvenciones obtenidas del Ministerio de Ciencia e Innovación.
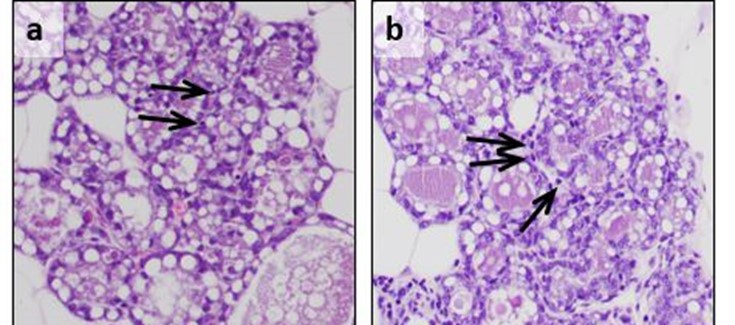
(*) Figura: microfotografías de corteshistológicos de glándulasmamarias de hembrasen el día 17,5 de gestación. (a) animal control; (b) animal con expresión de ERAS encélulasmioepiteliales. Observesecómo las célulasmioepitelialespresentannucleomegalia (mayor tamaño del núcleo) comoconsecuencia de la expression de ERAS (flechas).
Referencia del artículo:
Cancers 2021, 13(21), 5588; https://doi.org/10.3390/cancers13215588
ERAS, a Member of the Ras Superfamily, Acts as an Oncoprotein in the Mammary Gland
Autores: Cristian Suárez-Cabrera, Isabel Ojeda-Pérez, Raquel Sánchez-Baltasar, Angustias Page, Ana Bravo, Manuel Navarro y Ángel Ramírez.
https://www.mdpi.com/2072-6694/13/21/5588